თანამედროვე PRP: "კლინიკური PRP"
ბოლო 10 წლის განმავლობაში PRP-ის მკურნალობის სქემამ დიდი ცვლილებები განიცადა.ექსპერიმენტული და კლინიკური კვლევების საშუალებით, ჩვენ ახლა უკეთ გავიგეთ თრომბოციტების და სხვა უჯრედების ფიზიოლოგიის შესახებ.გარდა ამისა, რამდენიმე მაღალი ხარისხის სისტემურმა შეფასებამ, მეტა-ანალიზმა და რანდომიზებულმა კონტროლირებადმა კვლევამ აჩვენა PRP ბიოტექნოლოგიის ეფექტურობა მრავალ სამედიცინო სფეროში, მათ შორის დერმატოლოგიაში, კარდიოქირურგიაში, პლასტიკური ქირურგიაში, ორთოპედიულ ქირურგიაში, ტკივილის მართვაში, ხერხემლის დაავადებებში და სპორტულ მედიცინაში. .
PRP-ის ამჟამინდელი მახასიათებელია მისი აბსოლუტური თრომბოციტების კონცენტრაცია, რომელიც იცვლება PRP-ის საწყისი განსაზღვრებიდან (თრომბოციტების კონცენტრაციის ჩათვლით საბაზისო მნიშვნელობაზე მაღალი) 1 × 10 6/μL-ზე მეტზე ან დაახლოებით 5-ჯერ თრომბოციტების მინიმალურ კონცენტრაციაზე თრომბოციტებში. საბაზისო.ფადადუს და სხვების ვრცელ მიმოხილვაში.შეფასდა 33 PRP სისტემა და პროტოკოლი.ზოგიერთი ამ სისტემის მიერ წარმოებული საბოლოო PRP პრეპარატის თრომბოციტების რაოდენობა უფრო დაბალია ვიდრე მთლიან სისხლში.მათ განაცხადეს, რომ PRP-ის თრომბოციტების კოეფიციენტი გაიზარდა 0,52-მდე ერთჯერადი ტრიალის ნაკრებით (Selphyl ®).ამის საპირისპიროდ, ორმაგი როტაციის EmCyte Genesis PurePRPII ® მოწყობილობის მიერ წარმოებული თრომბოციტების კონცენტრაცია ყველაზე მაღალია (1.6 × 10 6 / μL) .
ცხადია, ინ ვიტრო და ცხოველური მეთოდები არ არის იდეალური კვლევის გარემო კლინიკურ პრაქტიკაში წარმატებული ტრანსფორმაციისთვის.ანალოგიურად, მოწყობილობების შედარების კვლევა არ უჭერს მხარს გადაწყვეტილებას, რადგან ისინი აჩვენებს, რომ თრომბოციტების კონცენტრაცია PRP მოწყობილობებს შორის ძალიან განსხვავებულია.საბედნიეროდ, პროტეომიკაზე დაფუძნებული ტექნოლოგიისა და ანალიზის საშუალებით, ჩვენ შეგვიძლია გავზარდოთ ჩვენი გაგება უჯრედების ფუნქციების შესახებ PRP-ში, რაც გავლენას ახდენს მკურნალობის შედეგებზე.სტანდარტიზებული PRP პრეპარატებისა და ფორმულირებების შესახებ კონსენსუსის მიღწევამდე, PRP უნდა დაიცვას კლინიკური PRP ფორმულირებები, რათა ხელი შეუწყოს ქსოვილის აღდგენის მნიშვნელოვან მექანიზმებს და პროგრესულ კლინიკურ შედეგებს.
კლინიკური PRP ფორმულა
დღეისათვის ეფექტური კლინიკური PRP (C-PRP) ხასიათდება, როგორც აუტოლოგიური მრავალუჯრედიანი კომპონენტების კომპლექსური შემადგენლობა მცირე მოცულობის პლაზმაში, რომელიც მიიღება ცენტრიფუგაციის შემდეგ პერიფერიული სისხლის ნაწილიდან.ცენტრიფუგაციის შემდეგ, PRP და მისი არათრომბოციტების უჯრედების კომპონენტების აღდგენა შესაძლებელია კონცენტრაციის მოწყობილობიდან სხვადასხვა უჯრედის სიმკვრივის მიხედვით (რომელთაგან თრომბოციტების სიმკვრივე ყველაზე დაბალია).
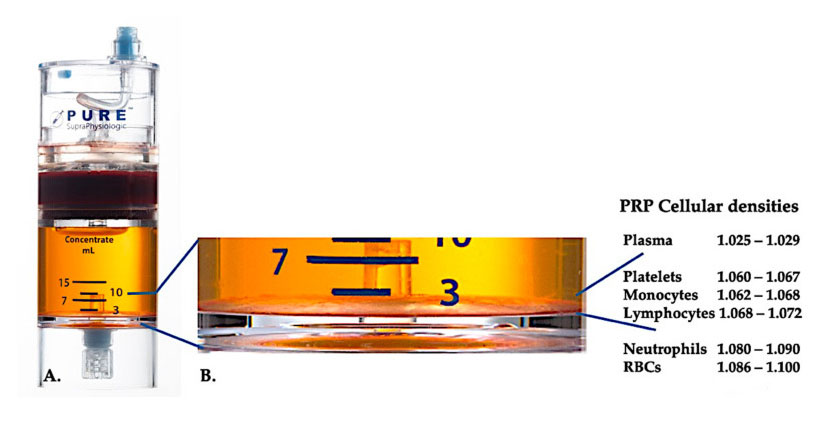
გამოიყენეთ PurePRP-SP ® უჯრედების სიმკვრივის გამიჯვნის მოწყობილობა (EmCyte Corporation, Fort Myers, FL, აშშ) გამოიყენებოდა მთლიანი სისხლისთვის ორი ცენტრიფუგაციის პროცედურის შემდეგ.ცენტრიფუგაციის პირველი პროცესის შემდეგ, მთლიანი სისხლის კომპონენტი გაიყო ორ ძირითად ფენად, თრომბოციტების (მჭლე) პლაზმური სუსპენზია და სისხლის წითელი უჯრედების შრე.A-ში დასრულებულია ცენტრიფუგაციის მეორე ეტაპი.PRP-ის რეალური მოცულობა შეიძლება ამოღებულ იქნეს პაციენტის გამოყენებისთვის.B-ში გადიდება აჩვენებს, რომ აღჭურვილობის ბოლოში არის ორგანიზებული მრავალკომპონენტიანი ერითროციტების დანალექი ყავისფერი ფენა (გამოსახული ლურჯი ხაზით), რომელიც შეიცავს თრომბოციტების, მონოციტების და ლიმფოციტების მაღალ კონცენტრაციას სიმკვრივის გრადიენტზე დაყრდნობით.ამ მაგალითში, ცუდი ნეიტროფილებით C-PRP მომზადების პროტოკოლის მიხედვით, ნეიტროფილების მინიმალური პროცენტი (<0.3%) და ერითროციტები (<0.1%) გამოიყოფა.
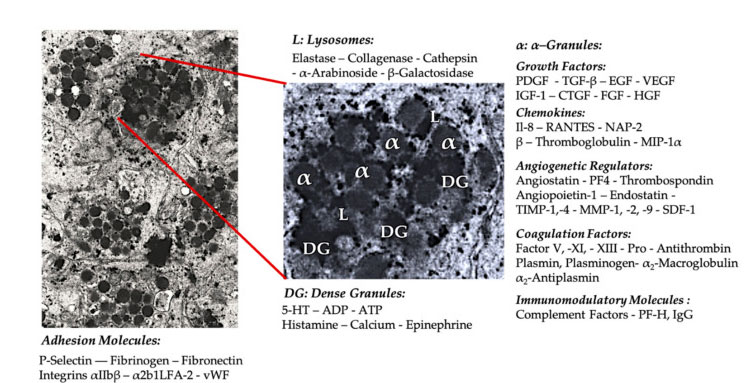
თრომბოციტების გრანულები
ადრეული კლინიკური PRP განაცხადის დროს, α- გრანულები ყველაზე ხშირად ციტირებულნი არიან თრომბოციტების შიდა სტრუქტურაში, რადგან ისინი შეიცავენ კოაგულაციის ფაქტორებს, დიდი რაოდენობით PDGF და ანგიოგენურ რეგულატორებს, მაგრამ აქვთ მცირე თრომბოგენური ფუნქცია.სხვა ფაქტორები მოიცავს ნაკლებად ცნობილ ქიმიოკინს და ციტოკინის კომპონენტებს, როგორიცაა თრომბოციტების ფაქტორი 4 (PF4), თრომბოციტების წინა ძირითადი ცილა, P-სელექტინი (ინტეგრინის აქტივატორი) და ქემოკინი RANTES (რეგულირდება აქტივაციით, გამოხატავს ნორმალურ T უჯრედებს და სავარაუდოდ. გამოყოფა).ამ სპეციფიკური თრომბოციტების გრანულების კომპონენტების საერთო ფუნქციაა სხვა იმუნური უჯრედების რეკრუტირება და გააქტიურება ან ენდოთელური უჯრედების ანთების გამოწვევა.
მკვრივი მარცვლოვანი კომპონენტები, როგორიცაა ADP, სეროტონინი, პოლიფოსფატი, ჰისტამინი და ადრენალინი, უფრო ნათლად გამოიყენება, როგორც თრომბოციტების აქტივაციისა და თრომბოზის რეგულატორები.რაც მთავარია, ამ ელემენტთაგან ბევრს აქვს იმუნური უჯრედების მოდიფიცირების ფუნქცია.თრომბოციტების ADP აღიარებულია P2Y12ADP რეცეპტორით დენდრიტულ უჯრედებზე (DC), რაც ზრდის ანტიგენის ენდოციტოზს.DC (ანტიგენის წარმდგენი უჯრედი) ძალიან მნიშვნელოვანია T უჯრედების იმუნური პასუხის დასაწყებად და დამცავი იმუნური პასუხის გასაკონტროლებლად, რომელიც აკავშირებს თანდაყოლილ იმუნურ სისტემასა და ადაპტირებულ იმუნურ სისტემას.გარდა ამისა, თრომბოციტების ადენოზინტრიფოსფატი (ATP) აგზავნის სიგნალებს T უჯრედების P2X7 რეცეპტორის მეშვეობით, რაც იწვევს CD4 T დამხმარე უჯრედების დიფერენციაციას პროანთებით T დამხმარე 17 (Th17) უჯრედებად.სხვა თრომბოციტების მკვრივი გრანულების კომპონენტები (როგორიცაა გლუტამატი და სეროტონინი) იწვევენ T უჯრედების მიგრაციას და ზრდის მონოციტების დიფერენციაციას DC-მდე, შესაბამისად.PRP-ში, მკვრივი ნაწილაკებისგან მიღებული ეს იმუნომოდულატორები ძალიან გამდიდრებულია და აქვთ მნიშვნელოვანი იმუნური ფუნქციები.
თრომბოციტებსა და სხვა (რეცეპტორულ) უჯრედებს შორის პირდაპირი და არაპირდაპირი პოტენციური ურთიერთქმედების რაოდენობა ფართოა.ამიტომ, PRP-ის გამოყენება ადგილობრივ პათოლოგიურ ქსოვილოვან გარემოში შეიძლება გამოიწვიოს სხვადასხვა ანთებითი ეფექტი.
თრომბოციტების კონცენტრაცია
C-PRP უნდა შეიცავდეს კონცენტრირებული თრომბოციტების კლინიკურ დოზებს, რათა მოხდეს სასარგებლო თერაპიული ეფექტი.C-PRP-ში თრომბოციტებმა უნდა გაააქტიურონ უჯრედების პროლიფერაცია, მეზენქიმული და ნეიროტროფიული ფაქტორების სინთეზი, ხელი შეუწყონ ქიმიოტაქსიური უჯრედების მიგრაციას და გაააქტიურონ იმუნორეგულაციური აქტივობა, როგორც ეს ნაჩვენებია სურათზე.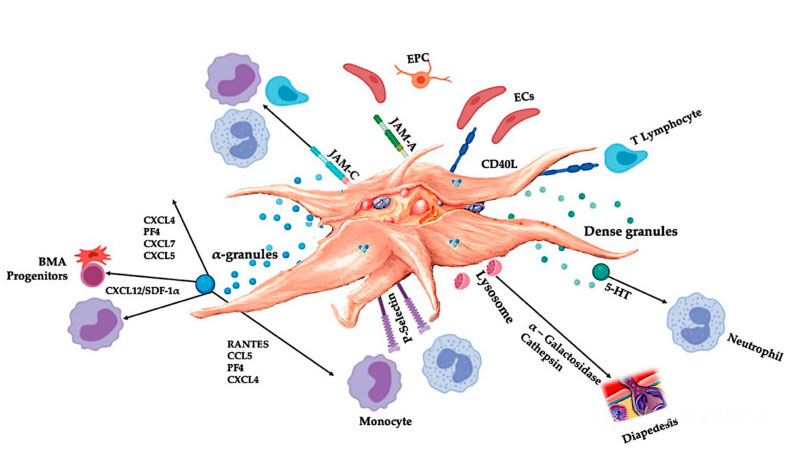
გააქტიურებული თრომბოციტები, PGF და ადჰეზიური მოლეკულების გამოყოფა შუამავლობს სხვადასხვა უჯრედულ ურთიერთქმედებას: ქიმიოტაქსის, უჯრედების ადჰეზიას, მიგრაციას და უჯრედების დიფერენციაციას და არეგულირებს იმუნურ მარეგულირებელ აქტივობებს.ეს თრომბოციტების უჯრედის ურთიერთქმედება ხელს უწყობს ანგიოგენეზს და ანთებით აქტივობას და საბოლოოდ ასტიმულირებს ქსოვილის აღდგენის პროცესს.აბრევიატურები: BMA: ძვლის ტვინის ასპირატი, EPC: ენდოთელური პროგენიტორული უჯრედები, EC: ენდოთელური უჯრედები, 5-HT: 5-ჰიდროქსიტრიპტამინი, RANTES: T უჯრედების ნორმალური ექსპრესიის გააქტიურებული რეგულირება და სავარაუდო სეკრეცია, JAM: შეერთების ადჰეზიური მოლეკულის ტიპი, CD40L: 40 ლიგანდი, SDF-1 α: სტრომული უჯრედებიდან მიღებული ფაქტორი-1 α, CXCL: ქიმიოკინის (CXC მოტივი) ლიგანდი, PF4: თრომბოციტების ფაქტორი 4. ადაპტირებულია Everts et al.
მარქსი იყო პირველი ადამიანი, ვინც დაამტკიცა, რომ ძვლებისა და რბილი ქსოვილების შეხორცება გაუმჯობესდა და თრომბოციტების მინიმალური რაოდენობა იყო 1 × 10 6 / μL. 1.3 × 106 თრომბოციტების/μL-ზე, ამ კვლევამ აჩვენა მეტი შერწყმა.გარდა ამისა, გიუსტი და სხვ.გამოვლინდა 1,5 × ქსოვილის აღდგენის მექანიზმი 109 დოზით მოითხოვს თრომბოციტებს/მლ ენდოთელური უჯრედების აქტივობის მეშვეობით ფუნქციური ანგიოგენეზის ინდუცირებისთვის.ამ უკანასკნელ კვლევაში, უფრო მაღალი კონცენტრაცია ამცირებს თრომბოციტების ანგიოგენეზის პოტენციალს ფოლიკულებში და მის გარშემო.გარდა ამისა, ადრეულმა მონაცემებმა აჩვენა, რომ PRP-ის დოზა ასევე იმოქმედებს მკურნალობის შედეგებზე.ამიტომ, ანგიოგენეზის რეაქციის მნიშვნელოვანი ინდუცირებისთვის და უჯრედების პროლიფერაციისა და უჯრედების მიგრაციის სტიმულირებისთვის, C-PRP უნდა შეიცავდეს მინიმუმ 7.5 5 მლ PRP სამკურნალო ბოთლში × 10 9 შეუძლია თრომბოციტების მიწოდება.
გარდა დოზაზე დამოკიდებულებისა, PRP-ის ეფექტი უჯრედების აქტივობაზე, როგორც ჩანს, ძალიან დროზეა დამოკიდებული.სოფო და სხვ.ეს შედეგები ვარაუდობს, რომ ადამიანის თრომბოციტების ლიზატებთან მოკლევადიანი ზემოქმედება შეუძლია ძვლის უჯრედების პროლიფერაციისა და ქიმიოტაქსის სტიმულირება.პირიქით, PRP-ზე ხანგრძლივი ზემოქმედება გამოიწვევს ტუტე ფოსფატაზის და მინერალების წარმოქმნას.
სისხლის წითელი უჯრედი
სისხლის წითელი უჯრედები პასუხისმგებელნი არიან ქსოვილებში ჟანგბადის გადატანაზე და ქსოვილებიდან ფილტვებში ნახშირორჟანგის გადატანაზე.მათ არ აქვთ ბირთვი და შედგება ჰემის მოლეკულებისგან, რომლებიც აკავშირებენ ცილებს.რკინა და ჰემის კომპონენტები სისხლის წითელ უჯრედებში ხელს უწყობს ჟანგბადის და ნახშირორჟანგის კომბინაციას.ზოგადად, სისხლის წითელი უჯრედების სიცოცხლის ციკლი დაახლოებით 120 დღეა.ისინი გამოიყოფა ცირკულაციისგან მაკროფაგების მიერ სისხლის წითელი უჯრედების დაბერების პროცესით.PRP ნიმუშებში სისხლის წითელი უჯრედები შეიძლება დაზიანდეს ათვლის პირობებში (მაგალითად, მთლიანი სისხლით სისხლდენის ოპერაცია, იმუნური შუამავლობით გამოწვეული პროცესი, ოქსიდაციური სტრესი ან არაადეკვატური PRP კონცენტრაციის სქემა).ამრიგად, სისხლის წითელი უჯრედის მემბრანა იშლება და ათავისუფლებს ტოქსიკურ ჰემოგლობინს (Hb), რომელიც იზომება პლაზმიდან თავისუფალი ჰემოგლობინის (PFH), ჰემისა და რკინით.].PFH და მისი დეგრადაციის პროდუქტები (ჰემი და რკინა) ერთობლივად იწვევს ქსოვილებზე მავნე და ციტოტოქსიურ ეფექტებს, რაც იწვევს ოქსიდაციურ სტრესს, აზოტის ოქსიდის დაკარგვას, ანთებითი გზების გააქტიურებას და იმუნოსუპრესიას.ეს ეფექტები საბოლოოდ გამოიწვევს მიკროცირკულაციის დისფუნქციას, ადგილობრივ ვაზოკონსტრიქციას და სისხლძარღვთა დაზიანებას, ასევე ქსოვილის სერიოზულ დაზიანებას.
ყველაზე მნიშვნელოვანი ის არის, რომ როდესაც C-PRP შემცველი RBC მიეწოდება ქსოვილს, ეს გამოიწვევს ადგილობრივ რეაქციას, რომელსაც ეწოდება ერიპტოზი, რაც გამოიწვევს ეფექტური ციტოკინის და მაკროფაგების მიგრაციის ინჰიბიტორის გამოყოფას.ეს ციტოკინი აფერხებს მონოციტებისა და მაკროფაგების მიგრაციას.ის აწვდის ძლიერ პრო-ანთებით სიგნალებს მიმდებარე ქსოვილებზე, აფერხებს ღეროვანი უჯრედების მიგრაციას და ფიბრობლასტების პროლიფერაციას და იწვევს ლოკალური უჯრედების მნიშვნელოვან დისფუნქციას.აქედან გამომდინარე, მნიშვნელოვანია შეზღუდოს RBC დაბინძურება PRP პრეპარატებში.გარდა ამისა, სისხლის წითელი უჯრედების როლი ქსოვილების რეგენერაციაში არასოდეს ყოფილა განსაზღვრული.ადექვატური C-PRP ცენტრიფუგაცია და მომზადების პროცესი ჩვეულებრივ შეამცირებს ან თუნდაც აღმოფხვრის სისხლის წითელი უჯრედების არსებობას, რითაც თავიდან აიცილებს ჰემოლიზისა და პოლიციტემიის უარყოფით შედეგებს.
ლეიკოციტები C-PRP-ში
PRP პრეპარატებში სისხლის თეთრი უჯრედების არსებობა დამოკიდებულია სამკურნალო აღჭურვილობასა და მომზადების სქემაზე.პლაზმაზე დაფუძნებულ PRP აღჭურვილობაში სისხლის თეთრი უჯრედები მთლიანად აღმოიფხვრება;თუმცა, სისხლის თეთრი უჯრედები მნიშვნელოვნად იყო კონცენტრირებული ერითროციტების დალექვის ყავისფერი შრის PRP მომზადებაში.მისი იმუნური და მასპინძლის დამცავი მექანიზმების გამო, სისხლის თეთრი უჯრედები დიდ გავლენას ახდენენ ქსოვილის მწვავე და ქრონიკული მდგომარეობის შიდა ბიოლოგიაზე.ეს მახასიათებლები უფრო დეტალურად იქნება განხილული ქვემოთ.ამიტომ, სპეციფიკური ლეიკოციტების არსებობა C-PRP-ში შეიძლება გამოიწვიოს მნიშვნელოვანი უჯრედული და ქსოვილოვანი ეფექტები.უფრო კონკრეტულად, PRP ერითროციტების დალექვის სხვადასხვა ყავისფერ-ყვითელი შრის სისტემები იყენებენ სხვადასხვა მომზადების სქემებს, რითაც გამოიმუშავებენ ნეიტროფილების, ლიმფოციტების და მონოციტების სხვადასხვა პროპორციას PRP-ში.ეოზინოფილების და ბაზოფილების გაზომვა შეუძლებელია PRP-ის პრეპარატებში, რადგან მათი უჯრედის მემბრანები ზედმეტად მყიფეა, რათა გაუძლოს ცენტრიდანული დამუშავების ძალებს.
ნეიტროფილები
ნეიტროფილები არის აუცილებელი ლეიკოციტები სამკურნალო მრავალ გზაზე.ეს გზები ერწყმის თრომბოციტებში არსებულ ანტიმიკრობულ პროტეინებს და ქმნის მკვრივ ბარიერს ინვაზიური პათოგენების წინააღმდეგ.ნეიტროფილების არსებობა განისაზღვრება C-PRP-ის მკურნალობის მიზნის მიხედვით.ქსოვილის ანთების გაზრდილი დონე შეიძლება საჭირო გახდეს ქრონიკული ჭრილობის მოვლის PRP ბიოთერაპიისას ან ძვლის ზრდისა და შეხორცებისკენ მიმართული აპლიკაციებში.მნიშვნელოვანია, რომ ნეიტროფილების დამატებითი ფუნქციები იქნა ნაპოვნი რამდენიმე მოდელში, რაც ხაზს უსვამს მათ როლს ანგიოგენეზსა და ქსოვილების აღდგენაში.თუმცა, ნეიტროფილებს ასევე შეუძლიათ გამოიწვიონ მავნე ზემოქმედება, ამიტომ ისინი არ არის შესაფერისი ზოგიერთი გამოყენებისთვის.ჟოუმ და ვანგმა დაადასტურეს, რომ ნეიტროფილებით მდიდარი PRP-ის გამოყენებამ შეიძლება გამოიწვიოს III ტიპის კოლაგენის და I ტიპის კოლაგენის თანაფარდობის გაზრდა, რითაც გაამწვავებს ფიბროზი და ამცირებს მყესების სიმტკიცეს.ნეიტროფილების შუამავლობით გამოწვეული სხვა მავნე მახასიათებელია ანთებითი ციტოკინების და მატრიქსის მეტალოპროტეინაზების (MMPs) გამოყოფა, რომელსაც შეუძლია ხელი შეუწყოს ანთებას და კატაბოლიზმს ქსოვილებზე გამოყენებისას.
ლეიკომონოციტი
C-PRP-ში, მონონუკლეარული T და B ლიმფოციტები უფრო კონცენტრირებულია, ვიდრე ნებისმიერი სხვა სისხლის თეთრი უჯრედი.ისინი მჭიდრო კავშირშია უჯრედის შუამავლობით ციტოტოქსიურ ადაპტაციურ იმუნიტეტთან.ლიმფოციტებს შეუძლიათ გამოიწვიონ უჯრედული რეაქციები ინფექციასთან საბრძოლველად და დამპყრობლებთან ადაპტაციისთვის.გარდა ამისა, T-ლიმფოციტებით მიღებული ციტოკინები (ინტერფერონ-γ [IFN-γ] და ინტერლეუკინ-4 (IL-4) აძლიერებენ მაკროფაგების პოლარიზაციას. Verassar et al. დადასტურებულია, რომ ჩვეულებრივი T ლიმფოციტებს შეუძლიათ ირიბად ხელი შეუწყონ ქსოვილების შეხორცებას. თაგვის მოდელი მონოციტების და მაკროფაგების დიფერენციაციის რეგულირებით.
მონოციტი - მულტიპოტენტური აღდგენითი უჯრედი
გამოყენებული PRP მოსამზადებელი მოწყობილობის მიხედვით, PRP სამკურნალო ბოთლში მონოციტები შეიძლება გამოვიდეს ან არ არსებობდეს.სამწუხაროდ, მათი შესრულება და რეგენერაციის უნარი იშვიათად არის განხილული ლიტერატურაში.ამიტომ მონოციტებს მომზადების მეთოდში ან საბოლოო ფორმულაში მცირე ყურადღება ექცევა.მონოციტების ჯგუფი ჰეტეროგენულია, წარმოიქმნება ძვლის ტვინის წინამორბედი უჯრედებიდან და ტრანსპორტირდება პერიფერიულ ქსოვილებში ჰემატოპოეტური ღეროვანი უჯრედების გზით მიკროგარემოს სტიმულაციის მიხედვით.ჰომეოსტაზისა და ანთების დროს მოცირკულირე მონოციტები ტოვებენ სისხლის ნაკადს და გადადიან დაზიანებულ ან დეგრადირებულ ქსოვილებში.მათ შეუძლიათ იმოქმედონ როგორც მაკროფაგები (M Φ) ეფექტური უჯრედები ან პროგენიტორული უჯრედები.მონოციტები, მაკროფაგები და დენდრიტული უჯრედები წარმოადგენს მონობირთვულ ფაგოციტურ სისტემას (MPS). MPS-ის ტიპიური მახასიათებელია მისი გენის ექსპრესიის ნიმუშის პლასტიურობა და ამ ტიპის უჯრედებს შორის ფუნქციური გადახურვა.დეგენერირებულ ქსოვილებში რეზიდენტი მაკროფაგები, ადგილობრივად მოქმედი ზრდის ფაქტორები, პრო-ანთებითი ციტოკინები, აპოპტოზური ან ნეკროზული უჯრედები და მიკრობული პროდუქტები იწყებენ მონოციტების დიფერენცირებას MPS უჯრედების ჯგუფებად.დავუშვათ, რომ როდესაც C-PRP შემცველი მაღალი პროდუქტიულობის მონოციტები შეჰყავთ დაავადების ადგილობრივ მიკროგარემოში, მონოციტები სავარაუდოდ დიფერენცირდებიან M Φ-ად, რათა გამოიწვიონ ძირითადი უჯრედული ცვლილებები.
მონოციტიდან M Φ-მდე ტრანსფორმაციის პროცესში სპეციფიკური M Φ ფენოტიპი.ბოლო ათი წლის განმავლობაში შემუშავდა მოდელი, რომელიც აერთიანებს M Φ აქტივაციის რთული მექანიზმი აღწერილია როგორც ორი საპირისპირო მდგომარეობის პოლარიზაცია: M Φ ფენოტიპი 1 (M Φ 1, კლასიკური აქტივაცია) და M Φ ფენოტიპი 2 (M Φ). 2, ალტერნატიული გააქტიურება).M Φ 1 ხასიათდება ანთებითი ციტოკინის სეკრეციით (IFN-γ) და აზოტის ოქსიდით, რათა გამოიმუშაოს პათოგენის მკვლელობის ეფექტური მექანიზმი.M Φ ფენოტიპი ასევე წარმოქმნის სისხლძარღვთა ენდოთელური ზრდის ფაქტორს (VEGF) და ფიბრობლასტების ზრდის ფაქტორს (FGF).M Φ ფენოტიპი შედგება მაღალი ფაგოციტოზის მქონე ანთების საწინააღმდეგო უჯრედებისგან.M Φ 2 აწარმოებს უჯრედგარე მატრიქსის კომპონენტებს, ანგიოგენეზს და ქიმიოკინებს და ინტერლეუკინს 10 (IL-10).პათოგენის დაცვის გარდა, M Φ მას ასევე შეუძლია შეამციროს ანთება და ხელი შეუწყოს ქსოვილების აღდგენას.აღსანიშნავია, რომ M Φ 2 იყოფა M in vitro Φ 2a、M Φ 2b და M Φ 2. ეს დამოკიდებულია სტიმულზე.ამ ქვეტიპების in vivo თარგმნა რთულია, რადგან ქსოვილი შეიძლება შეიცავდეს შერეულ M Φ ჯგუფებს.საინტერესოა, რომ ადგილობრივი გარემოსდაცვითი სიგნალების და IL-4 დონის საფუძველზე, პროანთებითი M Φ 1 შეიძლება გარდაიქმნას M Φ 2-ის შეკეთების ხელშეწყობის მიზნით. შეიძლება ხელი შეუწყოს ქსოვილების უკეთეს აღდგენას, რადგან მათ აქვთ ანთების საწინააღმდეგო ქსოვილის აღდგენის და უჯრედული სიგნალის გადაცემის შესაძლებლობები.
სისხლის თეთრი უჯრედების ფრაქციის დაბნეული განმარტება PRP-ში
სისხლის თეთრი უჯრედების არსებობა PRP სამკურნალო ბოთლებში დამოკიდებულია PRP მომზადების მოწყობილობაზე და შეიძლება ჰქონდეს მნიშვნელოვანი განსხვავებები.არსებობს მრავალი დავა ლეიკოციტების არსებობის შესახებ და მათი წვლილი სხვადასხვა ქვეPRP პროდუქტებში (როგორიცაა PRGF, P-PRP, LP-PRP, LR-PRP, P-PRF და L-PRF). ბოლო მიმოხილვაში, ექვსი რანდომიზირებული კონტროლირებადი კვლევები (მტკიცებულების დონე 1) და სამი პერსპექტიული შედარებითი კვლევა (მტკიცებულების დონე 2) მოიცავდა 1055 პაციენტს, რაც მიუთითებს იმაზე, რომ LR-PRP და LP-PRP ჰქონდათ მსგავსი უსაფრთხოება.ავტორმა დაასკვნა, რომ PRP-ის გვერდითი რეაქცია შეიძლება პირდაპირ არ იყოს დაკავშირებული სისხლის თეთრი უჯრედების კონცენტრაციასთან.სხვა კვლევაში, LR-PRP-მ არ შეცვალა ანთებითი ინტერლეუკინი (IL-1) OA მუხლის β, IL-6, IL-8 და IL-17).ეს შედეგები მხარს უჭერს მოსაზრებას, რომ ლეიკოციტების როლი PRP-ის ბიოლოგიურ აქტივობაში in vivo შეიძლება წარმოიშვას თრომბოციტებსა და ლეიკოციტებს შორის ურთიერთქმედების შედეგად.ამ ურთიერთქმედებამ შეიძლება ხელი შეუწყოს სხვა ფაქტორების (როგორიცაა ლიპოქსიგენი) ბიოსინთეზს, რამაც შეიძლება შეცვალოს ან ხელი შეუწყოს ანთების რეგრესიას.ანთებითი მოლეკულების (არაქიდონის მჟავა, ლეიკოტრიენი და პროსტაგლანდინი) საწყისი გამოთავისუფლების შემდეგ ლიპოქსიგენი A4 გამოიყოფა გააქტიურებული თრომბოციტებიდან ნეიტროფილების აქტივაციის თავიდან ასაცილებლად.სწორედ ამ გარემოშია, რომ M Φ ფენოტიპი M Φ 1-დან გადადის M Φ 2-ზე. გარდა ამისა, არსებობს მზარდი მტკიცებულება, რომ მოცირკულირე მონონუკლეარული უჯრედები შეიძლება დიფერენცირდნენ სხვადასხვა არაფაგოციტურ უჯრედებად მათი პლურიპოტენციის გამო.
PRP-ის ტიპი გავლენას მოახდენს MSC კულტურაზე.სუფთა PRP ან PPP ნიმუშებთან შედარებით, LR-PRP-ს შეუძლია გამოიწვიოს ძვლის ტვინიდან მიღებული MSC-ების (BMMSCs) მნიშვნელოვნად უფრო მაღალი პროლიფერაცია, უფრო სწრაფი გათავისუფლებით და უკეთესი PGF ბიოლოგიური აქტივობით.ყველა ეს მახასიათებელი ხელს უწყობს PRP სამკურნალო ბოთლში მონოციტების დამატებას და მათი იმუნომოდულატორული შესაძლებლობების და დიფერენცირების პოტენციალის აღიარებას.
PRP-ის თანდაყოლილი და ადაპტური იმუნური რეგულირება
თრომბოციტების ყველაზე ცნობილი ფიზიოლოგიური ფუნქციაა სისხლდენის კონტროლი.ისინი გროვდება ქსოვილის დაზიანების ადგილზე და დაზიანებულ სისხლძარღვებში.ეს მოვლენები გამოწვეულია ინტეგრინისა და სელექტინების ექსპრესიით, რომლებიც ასტიმულირებენ თრომბოციტების ადჰეზიას და აგრეგაციას.დაზიანებული ენდოთელიუმი კიდევ უფრო ამძიმებს ამ პროცესს და გამოვლენილი კოლაგენი და სხვა სუბენდოთელური მატრიქსის ცილები ხელს უწყობს თრომბოციტების ღრმა გააქტიურებას.ამ შემთხვევებში დადასტურდა ფონ ვილბრანდის ფაქტორსა (vWF) და გლიკოპროტეინს (GP), განსაკუთრებით GP-Ib-ს შორის ურთიერთქმედების მნიშვნელოვანი როლი.თრომბოციტების გააქტიურების შემდეგ, თრომბოციტების α-、 მკვრივი, ლიზოსომა და T- გრანულები არეგულირებს ეგზოციტოზს და ათავისუფლებს მათ შიგთავსს უჯრედგარე გარემოში.
თრომბოციტების გადაბმის მოლეკულა
იმისათვის, რომ უკეთ გავიგოთ PRP-ის როლი ანთებით ქსოვილებში და თრომბოციტებში იმუნურ პასუხში, უნდა გვესმოდეს, თუ როგორ შეუძლიათ სხვადასხვა თრომბოციტების ზედაპირის რეცეპტორებმა (ინტეგრინები) და შეერთების ადჰეზიის მოლეკულები (JAM) და უჯრედების ურთიერთქმედება, დაიწყოს კრიტიკული პროცესები თანდაყოლილ და ადაპტირებულ იმუნიტეტში.
ინტეგრინები არის უჯრედის ზედაპირის ადჰეზიური მოლეკულები, რომლებიც გვხვდება სხვადასხვა ტიპის უჯრედებში და გამოხატულია დიდი რაოდენობით თრომბოციტებზე.ინტეგრინებს მიეკუთვნება a5b1, a6b1, a2b1 LFA-2, (GPIa/IIa) და aIIbb3 (GPIIb/IIIa).ჩვეულებრივ, ისინი არსებობენ სტატიკური და დაბალი აფინურობის მდგომარეობაში.გააქტიურების შემდეგ ისინი გადადიან ლიგანდის შებოჭვის მაღალი აფინურობის მდგომარეობაზე.ინტეგრინებს აქვთ სხვადასხვა ფუნქციები თრომბოციტებზე და მონაწილეობენ თრომბოციტების ურთიერთქმედებაში რამდენიმე ტიპის სისხლის თეთრი უჯრედებთან, ენდოთელურ უჯრედებთან და უჯრედგარე მატრიქსთან.გარდა ამისა, GP-Ib-V-IX კომპლექსი გამოხატულია თრომბოციტების მემბრანაზე და წარმოადგენს ფონ vWF-თან შეკავშირების მთავარ რეცეპტორს.ეს ურთიერთქმედება შუამავლობს თავდაპირველ კონტაქტს თრომბოციტებსა და დაუცველ სუბენდოთელურ სტრუქტურებს შორის.თრომბოციტების ინტეგრინი და GP კომპლექსი დაკავშირებულია სხვადასხვა ანთებით პროცესებთან და მნიშვნელოვან როლს ასრულებს თრომბოციტ-ლეიკოციტური კომპლექსის ფორმირებაში.კერძოდ, ინტეგრინი aIIbb3 აუცილებელია სტაბილური კომპლექსის შესაქმნელად ფიბრინოგენის მაკროფაგ 1 ანტიგენის (Mac-1) რეცეპტორთან შერწყმით ნეიტროფილებზე.
თრომბოციტები, ნეიტროფილები და სისხლძარღვთა ენდოთელური უჯრედები გამოხატავენ სპეციფიკურ ადჰეზიურ მოლეკულებს, რომელსაც სელექტინი ეწოდება.ანთებით პირობებში თრომბოციტები გამოხატავს P-სელექტინს და ნეიტროფილის L-სელექტინს.თრომბოციტების გააქტიურების შემდეგ, P-სელექტინი შეიძლება დაუკავშირდეს ლიგანდს PSGL-1, რომელიც არსებობს ნეიტროფილებსა და მონოციტებზე.გარდა ამისა, PSGL-1-ის შეკავშირება იწყებს უჯრედშიდა სიგნალის კასკადურ რეაქციას, რომელიც ააქტიურებს ნეიტროფილებს ნეიტროფილების ინტეგრინის Mac-1 და ლიმფოციტების ფუნქციასთან დაკავშირებული ანტიგენის 1 (LFA-1) მეშვეობით.გააქტიურებული Mac-1 აკავშირებს GPIb ან GPIIb/IIIa თრომბოციტებზე ფიბრინოგენის მეშვეობით, რითაც სტაბილიზდება ნეიტროფილებსა და თრომბოციტებს შორის ურთიერთქმედება.გარდა ამისა, გააქტიურებული LFA-1 შეიძლება გაერთიანდეს თრომბოციტების უჯრედშორისი ადჰეზიის მოლეკულასთან 2, ნეიტროფილ-თრომბოციტების კომპლექსის შემდგომი სტაბილიზაციისთვის, რათა ხელი შეუწყოს უჯრედებთან ხანგრძლივ ადჰეზიას.
თრომბოციტები და ლეიკოციტები მთავარ როლს თამაშობენ თანდაყოლილ და ადაპტირებულ იმუნურ პასუხებში
სხეულს შეუძლია ამოიცნოს უცხო სხეულები და დაზიანებული ქსოვილები მწვავე ან ქრონიკული დაავადებების დროს, რათა დაიწყოს ჭრილობების შეხორცების კასკადური რეაქცია და ანთებითი გზა.თანდაყოლილი და ადაპტური იმუნური სისტემა იცავს მასპინძელს ინფექციისგან და სისხლის თეთრი უჯრედები მნიშვნელოვან როლს ასრულებენ ორ სისტემას შორის გადახურვაში.კონკრეტულად, მონოციტები, მაკროფაგები, ნეიტროფილები და ბუნებრივი მკვლელი უჯრედები მთავარ როლს ასრულებენ თანდაყოლილ სისტემაში, ხოლო ლიმფოციტები და მათი ქვეჯგუფები მსგავს როლს ასრულებენ ადაპტაციურ იმუნურ სისტემაში.
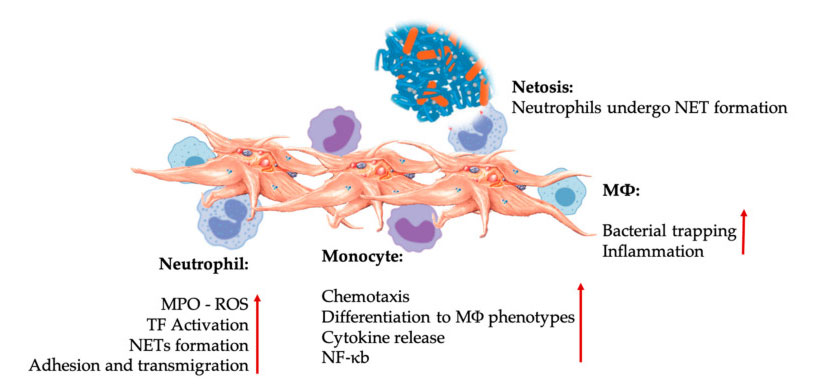
თრომბოციტების და ლეიკოციტების ურთიერთქმედება თანდაყოლილი იმუნური უჯრედების ურთიერთქმედებებში.თრომბოციტები ურთიერთქმედებენ ნეიტროფილებთან და მონოციტებთან და ბოლოს M Φ-თან ურთიერთქმედებენ, არეგულირებენ და ზრდიან მათ ეფექტურ ფუნქციებს.ეს თრომბოციტები-ლეიკოციტების ურთიერთქმედება იწვევს ანთებას სხვადასხვა მექანიზმების მეშვეობით, მათ შორის NETosis.აბრევიატურები: MPO: მიელოპეროქსიდაზა, ROS: რეაქტიული ჟანგბადის სახეობები, TF: ქსოვილის ფაქტორი, NET: ნეიტროფილების უჯრედგარე ხაფანგი, NF-κ B: ბირთვული ფაქტორი კაპა B, M Φ: მაკროფაგები.
თანდაყოლილი იმუნური სისტემა
თანდაყოლილი იმუნური სისტემის როლი არის ინვაზიური მიკროორგანიზმების ან ქსოვილის ფრაგმენტების არასპეციფიკური იდენტიფიცირება და მათი კლირენსის სტიმულირება.როდესაც გარკვეული მოლეკულური სტრუქტურები, რომელსაც ეწოდება ზედაპირის გამოხატვის ნიმუშის ამოცნობის რეცეპტორები (PRRs) გაერთიანდება პათოგენთან დაკავშირებულ მოლეკულურ შაბლონებთან და დაზიანებასთან დაკავშირებულ მოლეკულურ ნიმუშებთან, თანდაყოლილი იმუნური სისტემა გააქტიურდება.არსებობს მრავალი სახის PRR, მათ შორის Toll-ის მსგავსი რეცეპტორები (TLR) და RIG-1 მსგავსი რეცეპტორები (RLR).ამ რეცეპტორებს შეუძლიათ გაააქტიურონ ტრანსკრიფციის მთავარი ფაქტორი კაპა B (NF-κ B) ის ასევე არეგულირებს თანდაყოლილი და ადაპტური იმუნური პასუხის მრავალ ასპექტს.საინტერესოა, რომ თრომბოციტები ასევე გამოხატავს სხვადასხვა სახის იმუნორეგულაციური რეცეპტორების მოლეკულებს მათ ზედაპირზე და ციტოპლაზმზე, როგორიცაა P-სელექტინი, ტრანსმემბრანული ცილის CD40 ლიგანდი (CD40L), ციტოკინები (როგორიცაა IL-1 β, TGF- β) და თრომბოციტების სპეციფიკური TLR. ამიტომ, თრომბოციტებს შეუძლიათ ურთიერთქმედება სხვადასხვა იმუნურ უჯრედებთან.
თრომბოციტების-თეთრი უჯრედების ურთიერთქმედება თანდაყოლილ იმუნიტეტში
როდესაც თრომბოციტები შედიან ან შედიან სისხლის ნაკადში ან ქსოვილში, თრომბოციტები არის ერთ-ერთი უჯრედი, რომელიც პირველ რიგში აღმოაჩენს ენდოთელიუმის დაზიანებას და მიკრობულ პათოგენებს.თრომბოციტების აგრეგაცია და ხელს უწყობს თრომბოციტების აგონისტების ADP, თრომბინის და vWF განთავისუფლებას, რაც იწვევს თრომბოციტების გააქტიურებას და თრომბოციტების ქიმიოკინის რეცეპტორების C, CC, CXC და CX3C გამოხატვას, რაც იწვევს თრომბოციტების ინფიცირებულ ადგილზე ან დაზიანებას.
თანდაყოლილი იმუნური სისტემა გენეტიკურად წინასწარ არის განსაზღვრული დამპყრობლების აღმოსაჩენად, როგორიცაა ვირუსები, ბაქტერიები, პარაზიტები და ტოქსინები, ან ქსოვილის ჭრილობები და ჭრილობები.ეს არის არასპეციფიკური სისტემა, რადგან ნებისმიერი პათოგენი იქნება იდენტიფიცირებული, როგორც უცხო ან არა თვითმყოფადი და სწრაფად ლოკალიზებულია.თანდაყოლილი იმუნური სისტემა ეყრდნობა ცილებისა და ფაგოციტების ერთობლიობას, რომლებიც აღიარებენ პათოგენების კარგად შენახულ მახასიათებლებს და სწრაფად ააქტიურებენ იმუნურ პასუხს, რათა დაეხმაროს დამპყრობლების აღმოფხვრას, მაშინაც კი, თუ მასპინძელი აქამდე არასოდეს ყოფილა გამოვლენილი კონკრეტული პათოგენების მიმართ.
ნეიტროფილები, მონოციტები და დენდრიტული უჯრედები ყველაზე გავრცელებული თანდაყოლილი იმუნური უჯრედებია სისხლში.მათი რეკრუტირება აუცილებელია ადექვატური ადრეული იმუნური პასუხისთვის.როდესაც PRP გამოიყენება რეგენერაციულ მედიცინაში, თრომბოციტების თეთრი უჯრედების ურთიერთქმედება არეგულირებს ანთებას, ჭრილობების შეხორცებას და ქსოვილების შეკეთებას.TLR-4 თრომბოციტებზე ასტიმულირებს თრომბოციტების ნეიტროფილების ურთიერთქმედებას, რაც არეგულირებს ეგრეთ წოდებულ ლეიკოციტების ოქსიდაციურ აფეთქებას ნეიტროფილებისგან რეაქტიული ჟანგბადის სახეობების (ROS) და მიელოპეროქსიდაზას (MPO) გამოყოფის რეგულირებით.გარდა ამისა, თრომბოციტების-ნეიტროფილებისა და ნეიტროფილების დეგრანულაციის ურთიერთქმედება იწვევს ნეიტროფილ-უჯრედული ხაფანგების (NETs) წარმოქმნას.NETs შედგება ნეიტროფილების ბირთვისა და სხვა ნეიტროფილების უჯრედშიდა შიგთავსისგან, რომელსაც შეუძლია ბაქტერიების დაჭერა და მათი მოკვლა NETosis-ის საშუალებით.NET-ების ფორმირება ნეიტროფილების მკვლელობის აუცილებელი მექანიზმია.
თრომბოციტების გააქტიურების შემდეგ, მონოციტებს შეუძლიათ მიგრირება დაავადებულ და დეგენერაციულ ქსოვილებში, სადაც ისინი ახორციელებენ ადჰეზიურ მოქმედებას და გამოყოფენ ანთებით მოლეკულებს, რომლებმაც შეიძლება შეცვალონ ქიმიოტაქსიური და პროტეოლიზური თვისებები.გარდა ამისა, თრომბოციტებს შეუძლიათ გამოიწვიონ მონოციტების NF-κ B აქტივაცია მონოციტების ეფექტური ფუნქციის რეგულირებისთვის, რაც არის ანთებითი რეაქციისა და იმუნური უჯრედების გააქტიურებისა და დიფერენციაციის მთავარი შუამავალი.თრომბოციტები შემდგომში ხელს უწყობენ მონოციტების ენდოგენური ოქსიდაციური აფეთქებას, რაც ხელს უწყობს ფაგოციტური პათოგენების განადგურებას.MPO-ს გამოყოფა შუამავლობს თრომბოციტ-მონოციტს CD40L-MAC-1-ს შორის პირდაპირი ურთიერთქმედებით.საინტერესოა, რომ როდესაც P-სელექტინი ააქტიურებს თრომბოციტებს ქსოვილის მწვავე და ქრონიკულ ანთებით პირობებში, თრომბოციტებიდან მიღებული ქიმიოკინები PF4, RANTES, IL-1 β და CXCL-12 შეუძლიათ თავიდან აიცილონ მონოციტების სპონტანური აპოპტოზი, მაგრამ ხელი შეუწყონ მათ დიფერენციაციას მაკროფაგებად.
ადაპტური იმუნური სისტემა
მას შემდეგ, რაც არასპეციფიკური თანდაყოლილი იმუნური სისტემა ამოიცნობს მიკრობული ან ქსოვილის დაზიანებას, სპეციფიური ადაპტური იმუნური სისტემა აითვისებს.ადაპტაციური სისტემები მოიცავს ანტიგენთან შემაკავშირებელ B ლიმფოციტებს (B უჯრედები) და ჩვეულებრივ T ლიმფოციტებს (Treg), რომლებიც კოორდინაციას უწევენ პათოგენების კლირენსს.T უჯრედები შეიძლება უხეშად დაიყოს დამხმარე T უჯრედებად (Th უჯრედები) და ციტოტოქსიურ T უჯრედებად (Tc უჯრედები, ასევე ცნობილი როგორც T მკვლელი უჯრედები).Th უჯრედები შემდგომში იყოფა Th1, Th2 და Th17 უჯრედებად, რომლებსაც აქვთ ძირითადი ფუნქციები ანთების დროს.Th უჯრედებს შეუძლიათ გამოიყოს პროანთებითი ციტოკინები (მაგ. IFN-γ, TNF-β) და რამდენიმე ინტერლეუკინი (მაგ., IL-17). ისინი განსაკუთრებით ეფექტურია უჯრედშიდა ვირუსისა და ბაქტერიული ინფექციის თავიდან ასაცილებლად. Th უჯრედები ასტიმულირებენ უჯრედების გამრავლებას და დიფერენციაციას იმუნური პასუხი Tc უჯრედები არის მოქმედი უჯრედები, რომლებსაც შეუძლიათ უჯრედშიდა და უჯრედგარე მიკროორგანიზმებისა და უჯრედების აღმოფხვრა.
საინტერესოა, რომ Th2 უჯრედები აწარმოებენ IL-4-ს და გავლენას ახდენენ M Φ პოლარიზაციაზე, M Φ მართვადი რეგენერაციაზე M Φ 2 ფენოტიპზე, ხოლო IFN-γ M Φ იცვლება ანთებით M Φ 1 ფენოტიპზე, რაც დამოკიდებულია ციტოკინების დოზაზე და დროზე.მას შემდეგ, რაც IL-4 გააქტიურდება, M Φ 2 იწვევს Treg უჯრედების დიფერენცირებას Th2 უჯრედებად და შემდეგ წარმოქმნის დამატებით IL-4-ს (დადებითი უკუკავშირის მარყუჟი).Th უჯრედები გარდაქმნის M Φ ფენოტიპს მიმართულია რეგენერაციული ფენოტიპისკენ ქსოვილოვანი წარმოშობის ბიოლოგიური აგენტების საპასუხოდ.ეს მექანიზმი ემყარება მტკიცებულებას, რომ Th უჯრედები მნიშვნელოვან როლს ასრულებენ ანთების კონტროლსა და ქსოვილების აღდგენაში.
თრომბოციტების თეთრი უჯრედების ურთიერთქმედება ადაპტაციურ იმუნიტეტში
ადაპტირებული იმუნური სისტემა იყენებს ანტიგენ-სპეციფიკურ რეცეპტორებს და ახსოვს ადრე შეხვედრილი პათოგენები და ანადგურებს მათ, როდესაც მასპინძელს ხვდება.თუმცა, ეს ადაპტური იმუნური რეაქციები ნელა განვითარდა.კონიასი და სხვ.ის გვიჩვენებს, რომ თრომბოციტების კომპონენტი ხელს უწყობს რისკის აღქმას და ქსოვილის აღდგენას, და რომ თრომბოციტებისა და ლეიკოციტების ურთიერთქმედება ხელს უწყობს ადაპტური იმუნური პასუხის გააქტიურებას.
ადაპტური იმუნური პასუხის დროს, თრომბოციტები ხელს უწყობენ მონოციტებისა და მაკროფაგების პასუხებს DC და NK უჯრედების მომწიფების გზით, რაც იწვევს T უჯრედების და B უჯრედების სპეციფიკურ პასუხებს.ამრიგად, თრომბოციტების გრანულების კომპონენტები პირდაპირ გავლენას ახდენენ ადაპტაციურ იმუნიტეტზე CD40L-ის გამოხატვით, მოლეკულა, რომელიც აუცილებელია ადაპტური იმუნური პასუხის რეგულირებისთვის.თრომბოციტები CD40L-ით არა მხოლოდ თამაშობენ როლს ანტიგენის პრეზენტაციაში, არამედ გავლენას ახდენენ T უჯრედების რეაქციაზე.ლიუ და სხვ.აღმოჩნდა, რომ თრომბოციტები კომპლექსურად არეგულირებენ CD4 T უჯრედების პასუხს.CD4 T უჯრედების ქვეჯგუფების ეს დიფერენციალური რეგულირება ნიშნავს, რომ თრომბოციტები ხელს უწყობენ CD4 T უჯრედების რეაგირებას ანთებით სტიმულებზე, რითაც წარმოქმნიან ძლიერ პრო-ანთებით და ანთების საწინააღმდეგო პასუხებს.
თრომბოციტები ასევე არეგულირებენ B უჯრედების შუამავლობით ადაპტირებულ რეაქციას მიკრობული პათოგენების მიმართ.ცნობილია, რომ CD40L გააქტიურებულ CD4 T უჯრედებზე გამოიწვევს B უჯრედების CD40, რაც უზრუნველყოფს მეორე სიგნალს, რომელიც საჭიროა T-უჯრედზე დამოკიდებული B ლიმფოციტების გააქტიურებისთვის, შემდგომი ალოტიპის გარდაქმნისთვის და B უჯრედების დიფერენციაციისა და პროლიფერაციისთვის.ზოგადად, შედეგები ნათლად აჩვენებს თრომბოციტების სხვადასხვა ფუნქციებს ადაპტაციურ იმუნიტეტში, რაც მიუთითებს იმაზე, რომ თრომბოციტები აკავშირებენ T უჯრედებსა და B უჯრედებს შორის ურთიერთქმედებას CD40-CD40L-ის მეშვეობით, რითაც აძლიერებს T-უჯრედზე დამოკიდებული B უჯრედების რეაქციას.გარდა ამისა, თრომბოციტები მდიდარია უჯრედის ზედაპირის რეცეპტორებით, რომლებსაც შეუძლიათ ხელი შეუწყონ თრომბოციტების აქტივაციას და გაათავისუფლონ დიდი რაოდენობით ანთებითი და ბიოლოგიურად აქტიური მოლეკულები, რომლებიც ინახება სხვადასხვა თრომბოციტების ნაწილაკებში, რაც გავლენას ახდენს თანდაყოლილ და ადაპტირებულ იმუნურ პასუხზე.
თრომბოციტებიდან მიღებული სეროტონინის გაფართოებული როლი PRP-ში
სეროტონინი (5-ჰიდროქსიტრიპტამინი, 5-HT) მნიშვნელოვან როლს ასრულებს ცენტრალურ ნერვულ სისტემაში (ცნს), ტკივილის ტოლერანტობის ჩათვლით.შეფასებულია, რომ ადამიანის 5-HT-ის უმეტესი ნაწილი წარმოიქმნება კუჭ-ნაწლავის ტრაქტში, შემდეგ კი სისხლის მიმოქცევაში, სადაც ის შეიწოვება თრომბოციტების მიერ სეროტონინის უკუმიტაცების გადამყვანის მეშვეობით და ინახება მკვრივ ნაწილაკებში მაღალი კონცენტრაციით (65 მმოლ/ლ).5-HT არის ცნობილი ნეიროტრანსმიტერი და ჰორმონი, რომელიც ხელს უწყობს სხვადასხვა ნეიროფსიქოლოგიური პროცესების რეგულირებას ცენტრალურ ნერვულ სისტემაში (ცენტრალური 5-HT).თუმცა, 5-HT-ის უმეტესობა არსებობს ცენტრალური ნერვული სისტემის გარეთ (პერიფერიული 5-HT) და ის მონაწილეობს მრავალი ორგანოს სისტემის სისტემური და ფიჭური ბიოლოგიური ფუნქციების რეგულირებაში, მათ შორის გულ-სისხლძარღვთა, ფილტვების, კუჭ-ნაწლავის, უროგენიტალური და თრომბოციტების ფუნქციური სისტემების ჩათვლით.5-HT აქვს კონცენტრაციაზე დამოკიდებული მეტაბოლიზმი სხვადასხვა ტიპის უჯრედებზე, მათ შორის ადიპოციტებზე, ეპითელურ უჯრედებსა და სისხლის თეთრი უჯრედებზე.პერიფერიული 5-HT ასევე არის ძლიერი იმუნური მოდულატორი, რომელსაც შეუძლია გაააქტიუროს ან დათრგუნოს ანთება და გავლენა მოახდინოს სხვადასხვა იმუნურ უჯრედებზე მისი სპეციფიკური 5-HT რეცეპტორის (5HTR) მეშვეობით.
HT-ის პარაკრინული და ავტოკრინული მექანიზმი
5-HT-ის აქტივობა შუამავალია მისი ურთიერთქმედებით 5HTR-ებთან, რომელიც არის სუპეროჯახი შვიდი წევრით (5-HT 1 – 7) და სულ მცირე 14 განსხვავებული რეცეპტორის ქვეტიპით, მათ შორის ახლახან აღმოჩენილი წევრი 5-HT 7, მისი პერიფერიული და ფუნქცია ტკივილის მართვაში.თრომბოციტების დეგრანულაციის პროცესში, გააქტიურებული თრომბოციტები გამოყოფენ დიდი რაოდენობით თრომბოციტებიდან წარმოებულ 5-HT-ს, რომელსაც შეუძლია ხელი შეუწყოს სისხლძარღვთა შეკუმშვას და ასტიმულირებს მეზობელი თრომბოციტებისა და ლიმფოციტების აქტივაციას 5-HTR-ის ექსპრესიის გზით ენდოთელიალურ უჯრედებზე, გლუვ კუნთოვან უჯრედებზე და. იმუნური უჯრედები.პაკალა და სხვ.შესწავლილი იქნა 5-HT-ის მიტოზური ეფექტი სისხლძარღვთა ენდოთელიალურ უჯრედებზე და განისაზღვრა დაზიანებული სისხლძარღვების ზრდის ხელშეწყობის პოტენციალი ანგიოგენეზის სტიმულირებით.როგორ რეგულირდება ეს პროცესები, ბოლომდე გასაგები არ არის, მაგრამ ის შეიძლება მოიცავდეს დიფერენციალურ ორმხრივ სიგნალის გზებს ქსოვილის მიკროსქემში სისხლძარღვთა ენდოთელური უჯრედების და გლუვი კუნთების უჯრედების, ფიბრობლასტების და იმუნური უჯრედების ფუნქციების რეგულირებისთვის ამ უჯრედებზე სპეციფიკური 5-HT რეცეპტორების მეშვეობით. .აღწერილია თრომბოციტების 5-HT-ის ავტოკრინული ფუნქცია თრომბოციტების აქტივაციის შემდეგ [REF].5-HT-ის გამოყოფა აძლიერებს თრომბოციტების გააქტიურებას და მოცირკულირე თრომბოციტების რეკრუტირებას, რაც იწვევს სიგნალის კასკადური რეაქციების გააქტიურებას და თრომბოციტების რეაქტიულობის მხარდამჭერ ეფექტორებს.
იმუნომოდულატორული 5-HT ეფექტი
უფრო და უფრო მეტი მტკიცებულება აჩვენებს, რომ სეროტონინს შეუძლია როლი შეასრულოს სხვადასხვა 5HTR-ში, როგორც იმუნური მოდულატორი.5HTR-ის მიხედვით, რომელიც გამოხატულია სხვადასხვა ლეიკოციტებში, რომლებიც მონაწილეობენ ანთებით რეაქციაში, თრომბოციტებიდან მიღებული 5-HT მოქმედებს როგორც იმუნური რეგულატორი როგორც თანდაყოლილ, ასევე ადაპტირებულ იმუნურ სისტემაში.5-HT-ს შეუძლია Treg-ის პროლიფერაციის სტიმულირება და B უჯრედების, ბუნებრივი მკვლელი უჯრედების და ნეიტროფილების ფუნქციების რეგულირება DC-ისა და მონოციტების ანთებით ადგილზე რეკრუტირებით.ბოლო კვლევებმა აჩვენა, რომ თრომბოციტებით მიღებული 5-HT შეუძლია დაარეგულიროს იმუნური უჯრედების ფუნქცია კონკრეტულ პირობებში.ამიტომ, C-PRP-ის გამოყენებით, თრომბოციტების კონცენტრაცია 1 × 10 6/μL-ზე მეტია, შეიძლება მნიშვნელოვნად დაეხმაროს 5-HT-ის კონცენტრაციის ტრანსპორტირებას დიდი თრომბოციტებიდან ქსოვილში.მიკროგარემოში, რომელიც ხასიათდება ანთებითი კომპონენტებით, PRP-ს შეუძლია ურთიერთქმედება რამდენიმე იმუნურ უჯრედთან, რომლებიც მნიშვნელოვან როლს ასრულებენ ამ პათოლოგიებში, რამაც შეიძლება გავლენა მოახდინოს კლინიკურ შედეგებზე.
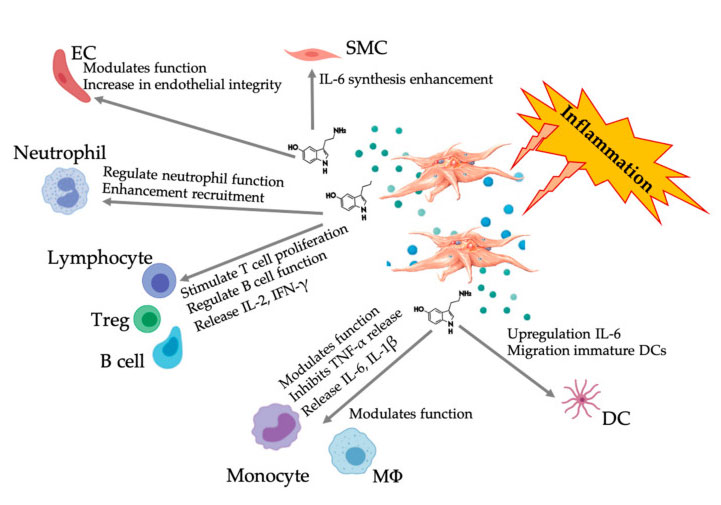
სურათი, რომელიც აჩვენებს მრავალმხრივ 5-HT პასუხს ანთებითი PRP თრომბოციტების გააქტიურების შემდეგ.თრომბოციტების გააქტიურების შემდეგ, თრომბოციტები ათავისუფლებენ გრანულებს, მათ შორის 5-HT მკვრივ გრანულებში, რომელსაც აქვს დიფერენციალური ეფექტის ფართო სპექტრი სხვადასხვა იმუნურ უჯრედებზე, ენდოთელიალურ უჯრედებზე და გლუვკუნთოვან უჯრედებზე.აბრევიატურები: SMC: გლუვი კუნთების უჯრედები, EC: ენდოთელური უჯრედები, Treg: ჩვეულებრივი T ლიმფოციტები, M Φ: მაკროფაგები, DC: დენდრიტული უჯრედები, IL: ინტერლეუკინი, IFN-γ: ინტერფერონი γ. მოდიფიცირებული და ადაპტირებულია Everts et al.და ჰალი და სხვ.
PRP-ის ტკივილგამაყუჩებელი ეფექტი
გააქტიურებული თრომბოციტები გამოყოფს ბევრ ანთების საწინააღმდეგო და ანთების საწინააღმდეგო შუამავალს, რომელსაც შეუძლია არა მხოლოდ გამოიწვიოს ტკივილი, არამედ შეამციროს ანთება და ტკივილი.გამოყენების შემდეგ, PRP-ის ტიპიური თრომბოციტების დინამიკა ცვლის მიკროგარემოს ქსოვილის შეკეთებამდე და რეგენერაციამდე სხვადასხვა კომპლექსური გზების მეშვეობით, რომლებიც დაკავშირებულია ანაბოლიზმთან და კატაბოლიზმთან, უჯრედების პროლიფერაციასთან, დიფერენციაციასთან და ღეროვანი უჯრედების რეგულირებასთან.PRP-ის ეს მახასიათებლები იწვევს PRP-ის გამოყენებას სხვადასხვა კლინიკურ პათოლოგიურ პირობებში, რომელიც ჩვეულებრივ ასოცირდება ქრონიკულ ტკივილთან (როგორიცაა სპორტული დაზიანება, ორთოპედიული დაავადება, ხერხემლის დაავადება და რთული ქრონიკული ჭრილობა), თუმცა ზუსტი მექანიზმი ბოლომდე დადგენილი არ არის.
2008 წელს ევერცი და სხვ.ეს არის პირველი რანდომიზებული კონტროლირებადი კვლევა, რომელშიც მოხსენებულია PRP პრეპარატის ტკივილგამაყუჩებელი ეფექტი, რომელიც მზადდება აუტოლოგიური ერითროციტების დალექვის სიჩქარის ყავისფერი შრისგან და აქტიურდება აუტოლოგიური თრომბინით მხრის ოპერაციის შემდეგ.მათ აღნიშნეს ვიზუალური ანალოგის მასშტაბის ქულების მნიშვნელოვანი შემცირება, ოპიოიდებზე დაფუძნებული ანალგეტიკების გამოყენება და უფრო წარმატებული პოსტოპერაციული რეაბილიტაცია.აღსანიშნავია, რომ ისინი ასახავს გააქტიურებული თრომბოციტების ტკივილგამაყუჩებელ ეფექტს და ვარაუდობენ თრომბოციტების 5-HT გამოთავისუფლების მექანიზმზე.მოკლედ, ახლად მომზადებულ PRP-ში თრომბოციტები მიძინებულია.თრომბოციტების პირდაპირ ან ირიბად გააქტიურების შემდეგ (ქსოვილის ფაქტორი), თრომბოციტები იცვლებიან ფორმას და წარმოქმნიან საკმარისად ცრუ თრომბოციტების აგრეგაციას.შემდეგ ისინი ათავისუფლებენ უჯრედშიდა α- და მკვრივ ნაწილაკებს.გააქტიურებული PRP-ით დამუშავებულ ქსოვილში შეიჭრება PGF, ციტოკინები და სხვა თრომბოციტების ლიზოსომები.უფრო კონკრეტულად, როდესაც მკვრივი ნაწილაკები ათავისუფლებენ შიგთავსს, ისინი გამოყოფენ დიდი რაოდენობით 5-HT-ს, რომელიც არეგულირებს ტკივილს.C-PRP-ში თრომბოციტების კონცენტრაცია 5-7-ჯერ მეტია ვიდრე პერიფერიულ სისხლში.ამიტომ, თრომბოციტებიდან 5-HT-ის გამოყოფა ასტრონომიულია.საინტერესოა, რომ Sprott et al.მოხსენებაში დაფიქსირდა, რომ ტკივილი მნიშვნელოვნად შემსუბუქდა აკუპუნქტურის და მოქსიბუსციის შემდეგ, თრომბოციტების წარმოებული 5-HT კონცენტრაცია მნიშვნელოვნად შემცირდა, შემდეგ კი 5-HT პლაზმური დონე გაიზარდა.
პერიფერიულ ნაწილში, თრომბოციტები, მასტოციტები და ენდოთელური უჯრედები გამოყოფენ ენდოგენურ 5-HT-ს ქსოვილის დაზიანების ან ქირურგიული ტრავმის დროს.საინტერესოა, რომ ნეირონების 5-HT რეცეპტორების მრავალფეროვნება გამოვლინდა პერიფერიულ არეში, რამაც დაადასტურა, რომ 5-HT შეიძლება ხელი შეუშალოს ნოციცეპციურ გადაცემას პერიფერიულ არეში.ეს კვლევები აჩვენებს, რომ 5-HT-ს შეუძლია გავლენა მოახდინოს პერიფერიული ქსოვილების ნოციცეპტურ გადაცემაზე 5-HT1, 5-HT2, 5-HT3, 5-HT4 და 5-HT7 რეცეპტორების მეშვეობით.
5-HT სისტემა წარმოადგენს ძლიერ სისტემას, რომელსაც შეუძლია შეამციროს და გაზარდოს ტკივილის ხარისხი მავნე სტიმულაციის შემდეგ.ქრონიკული ტკივილის მქონე პაციენტებში აღინიშნა ნოციცეპტური სიგნალების ცენტრალური და პერიფერიული რეგულირება და ცვლილებები 5-HT სისტემაში.ბოლო წლების განმავლობაში, კვლევების დიდი რაოდენობა ფოკუსირებულია 5-HT და მისი შესაბამისი რეცეპტორების როლზე მავნე ინფორმაციის დამუშავებასა და რეგულირებაში, რის შედეგადაც მიიღება ისეთი მედიკამენტები, როგორიცაა სეროტონინის უკუმიტაცების შერჩევითი ინჰიბიტორები (SSRI).ეს პრეპარატი თრგუნავს სეროტონინის უკუმიტაცებას პრესინაფსურ ნეირონებში სეროტონინის გამოთავისუფლების შემდეგ.ის გავლენას ახდენს სეროტონინის კომუნიკაციის ხანგრძლივობასა და ინტენსივობაზე და წარმოადგენს ქრონიკული ტკივილის ალტერნატიულ მკურნალობას.საჭიროა შემდგომი კლინიკური კვლევა, რათა ნათლად გავიგოთ PRP-დან მიღებული 5-HT ტკივილის რეგულირების მოლეკულური მექანიზმი ქრონიკულ და დეგენერაციულ დაავადებებში.
სხვა მონაცემები PRP-ის პოტენციური ტკივილგამაყუჩებელი ეფექტის გადასაჭრელად შეიძლება მიღებულ იქნას ტკივილგამაყუჩებელი ცხოველური მოდელის ტესტის შემდეგ.ამ მოდელებში შედარებითი სტატისტიკური დასკვნები რთულია, რადგან ეს კვლევები შეიცავს ძალიან ბევრ ცვლადს.მიუხედავად ამისა, ზოგიერთმა კლინიკურმა კვლევამ მიმართა PRP-ის ნოციცეპტიურ და ტკივილგამაყუჩებელ ეფექტებს.რამდენიმე კვლევამ აჩვენა, რომ პაციენტებს, რომლებიც მკურნალობენ ტენდინოზის ან მბრუნავი მანჟეტის ჭრილობისთვის, ნაკლებად ათავისუფლებენ ტკივილს.ამის საპირისპიროდ, რამდენიმე სხვა კვლევამ აჩვენა, რომ PRP-ს შეუძლია შეამციროს ან თუნდაც აღმოფხვრას ტკივილი მყესების დეგენერაციით, OA, პლანტარული ფაშიტიტით და ფეხის და ტერფის სხვა დაავადებებით.თრომბოციტების საბოლოო კონცენტრაცია და ბიოლოგიური უჯრედის შემადგენლობა იდენტიფიცირებულია, როგორც ძირითადი PRP მახასიათებლები, რომლებიც ხელს უწყობენ PRP-ის გამოყენების შემდეგ თანმიმდევრული ტკივილგამაყუჩებელი ეფექტის დაკვირვებას.სხვა ცვლადები მოიცავს PRP მიწოდების მეთოდს, გამოყენების ტექნოლოგიას, თრომბოციტების აქტივაციის პროტოკოლს, PGF-ის და ციტოკინების ბიოლოგიური აქტივობის დონეს, PRP გამოყენების ქსოვილის ტიპს და დაზიანების ტიპს.
აღსანიშნავია, რომ კუფლერმა გადაჭრა PRP-ის პოტენციალი ტკივილის შესამსუბუქებლად პაციენტებში მსუბუქი და მძიმე ქრონიკული ნეიროპათიური ტკივილით, დაზიანებული არარეგენერაციული ნერვის მეორადად.ამ კვლევის მიზანია გამოიკვლიოს შეიძლება თუ არა ნეიროპათიული ტკივილი შემცირდეს ან ჩაცხრება PRP-ის გამო, რომელიც ხელს უწყობს აქსონების რეგენერაციას და სამიზნე ნერვის რეინერვაციას.გასაკვირია, რომ პაციენტებს შორის, რომლებიც იღებენ მკურნალობას, ნეიროპათიური ტკივილი კვლავ აღმოიფხვრება ან შემსუბუქებულია ოპერაციიდან სულ მცირე ექვსი წლის შემდეგ.გარდა ამისა, ყველა პაციენტმა დაიწყო ტკივილის შემსუბუქება PRP-ის გამოყენებიდან სამი კვირის განმავლობაში.
ბოლო დროს მსგავსი ტკივილგამაყუჩებელი PRP ეფექტები შეინიშნება პოსტოპერაციული ჭრილობისა და კანის მოვლის სფეროში.საინტერესოა, რომ ავტორებმა აღნიშნეს ჭრილობის ტკივილის ფიზიოლოგიური ასპექტები, რომლებიც დაკავშირებულია სისხლძარღვთა დაზიანებასთან და კანის ქსოვილის ჰიპოქსიასთან.მათ ასევე განიხილეს ანგიოგენეზის მნიშვნელობა ჟანგბადის და საკვები ნივთიერებების მიწოდების ოპტიმიზაციაში.მათმა კვლევამ აჩვენა, რომ საკონტროლო ჯგუფთან შედარებით, პაციენტებს, რომლებიც იღებდნენ PRP მკურნალობას, ჰქონდათ ნაკლები ტკივილი და მნიშვნელოვნად გაიზარდა ანგიოგენეზი.საბოლოოდ, ჯოჰალმა და მისმა კოლეგებმა ჩაატარეს სისტემატური მიმოხილვა და მეტა-ანალიზი და დაასკვნეს, რომ PRP-ს შეუძლია შეამციროს ტკივილი PRP-ის გამოყენების შემდეგ ორთოპედიულ ჩვენებებში, განსაკუთრებით პაციენტებში, რომლებიც იღებენ გარე ეპიკონდილიტს და მუხლის OA მკურნალობას.სამწუხაროდ, ამ კვლევაში არ არის დაკონკრეტებული სისხლის თეთრი უჯრედების ეფექტები, თრომბოციტების კონცენტრაცია ან ეგზოგენური თრომბოციტების აქტივატორების გამოყენება, რადგან ეს ცვლადები გავლენას მოახდენს PRP-ის საერთო ეფექტურობაზე.PRP თრომბოციტების ოპტიმალური კონცენტრაცია ტკივილის მაქსიმალური შესამსუბუქებლად გაურკვეველია.ვირთხების ტენდინოზის მოდელში, თრომბოციტების კონცენტრაცია იყო 1.0 × 10 6 / μ At L, ტკივილი შეიძლება მთლიანად შემსუბუქდეს, ხოლო PRP-ით გამოწვეული ტკივილის შემსუბუქება თრომბოციტების კონცენტრაციის ნახევარით მნიშვნელოვნად შემცირდა.ამიტომ, ჩვენ მოვუწოდებთ უფრო მეტ კლინიკურ კვლევებს PRP-ის სხვადასხვა პრეპარატების ტკივილგამაყუჩებელი ეფექტების გამოსაკვლევად.
PRP და ანგიოგენეზის ეფექტი
C-PRP პრეპარატები ზუსტ რეგენერაციულ მედიცინაში იძლევა ბიომოლეკულების მიწოდებას, რომლებიც გამოიყოფა თრომბოციტების მაღალი კონცენტრაციით, რომლებიც გააქტიურებულია სამიზნე ქსოვილის უბნებზე.აქედან გამომდინარე, დაიწყო სხვადასხვა კასკადური რეაქციები, რომლებიც ხელს უწყობენ ადგილზე იმუნურ რეგულაციას, ანთებით პროცესს და ანგიოგენეზს, რათა ხელი შეუწყონ შეხორცებას და ქსოვილების აღდგენას.
ანგიოგენეზი არის დინამიური მრავალსაფეხურიანი პროცესი, რომელიც მოიცავს ჩანასახს და ქსოვილის მიკროსისხლძარღვებს ადრე არსებული სისხლძარღვებიდან.ანგიოგენეზი პროგრესირებს სხვადასხვა ბიოლოგიური მექანიზმების გამო, მათ შორის ენდოთელური უჯრედების მიგრაცია, პროლიფერაცია, დიფერენციაცია და დაყოფა.ეს უჯრედული პროცესები ახალი სისხლძარღვების წარმოქმნის წინაპირობაა.ისინი აუცილებელია უკვე არსებული სისხლძარღვების ზრდისთვის, სისხლის ნაკადის აღსადგენად და ქსოვილების აღდგენისა და ქსოვილების რეგენერაციის მაღალი მეტაბოლური აქტივობის მხარდასაჭერად.ეს ახალი სისხლძარღვები იძლევა ჟანგბადის და საკვები ნივთიერებების მიწოდებას და დამუშავებული ქსოვილებიდან ქვეპროდუქტების მოცილებას.
ანგიოგენეზის აქტივობა რეგულირდება ანგიოგენური ფაქტორი VEGF და ანტი-ანგიოგენური ფაქტორების სტიმულირებით (მაგ., ანგიოსტატინი და თრომბოსპონდინ-1 [TSP-1]).დაავადებულ და დეგრადირებულ მიკროგარემოში (მათ შორის დაბალი ჟანგბადის დაძაბულობა, დაბალი pH და მაღალი რძემჟავა დონე), ადგილობრივი ანგიოგენური ფაქტორები აღადგენს ანგიოგენეზის აქტივობას.
რამდენიმე თრომბოციტების ხსნად მედიას, როგორიცაა ძირითადი FGF და TGF-β და VEGF შეუძლია ენდოთელიუმის უჯრედების სტიმულირება ახალი სისხლძარღვების წარმოებისთვის.Landsdown-მა და Fortier-მა განაცხადეს PRP-ის შემადგენლობასთან დაკავშირებული სხვადასხვა შედეგები, მათ შორის მრავალი ანგიოგენური რეგულატორის ინტრათრომბოციტების წყაროები.გარდა ამისა, მათ დაასკვნეს, რომ ანგიოგენეზის ზრდა ხელს უწყობს MSK დაავადების შეხორცებას ცუდი სისხლძარღვების მქონე ადგილებში, როგორიცაა მენისკის რღვევა, მყესების დაზიანება და სხვა უბნები ცუდი ვასკულარიზაციის დროს.
თრომბოციტების ხელშემწყობი და ანტიანგიოგენური თვისებები
ბოლო რამდენიმე ათწლეულის განმავლობაში გამოქვეყნებულმა კვლევებმა დაამტკიცა, რომ თრომბოციტები მთავარ როლს ასრულებენ პირველადი ჰემოსტაზის, თრომბის წარმოქმნაში, ზრდის ფაქტორისა და ციტოკინის გამოთავისუფლებაში და ანგიოგენეზის რეგულირებაში, როგორც ქსოვილის აღდგენის პროცესის ნაწილი.პარადოქსულია, რომ PRP α- გრანულები შეიცავს პრო-ანგიოგენური ზრდის ფაქტორების, ანტი-ანგიოგენური პროტეინების და ციტოკინების არსენალს (როგორიცაა PF4, პლაზმინოგენის აქტივატორის ინჰიბიტორი-1 და TSP-1) და მიზნად ისახავს კონკრეტული ფაქტორების განთავისუფლებას, რომლებიც როლს ასრულებენ. .როლი ანგიოგენეზში.ამიტომ, PRP-ის როლი ანგიოგენეზის რეგულაციის კონტროლში შეიძლება განისაზღვროს უჯრედის ზედაპირის სპეციფიკური რეცეპტორების გააქტიურებით, TGF-β ინიცირებული პრო-ანგიოგენური და ანტიანგიოგენური რეაქციებით.თრომბოციტების უნარი განახორციელოს ანგიოგენეზის გზა დადასტურებულია პათოლოგიური ანგიოგენეზისა და სიმსივნური ანგიოგენეზის დროს.
თრომბოციტებიდან მიღებული ანგიოგენური ზრდის ფაქტორი და ანტიანგიოგენური ზრდის ფაქტორი, მიღებული α- და მკვრივი და წებოვანი მოლეკულებისგან.რაც მთავარია, ზოგადად მიღებულია, რომ თრომბოციტების საერთო ეფექტი ანგიოგენეზზე არის პრო-ანგიოგენური და მასტიმულირებელი.მოსალოდნელია, რომ PRP თერაპია გააკონტროლებს ანგიოგენეზის ინდუქციას, რაც ხელს შეუწყობს მრავალი დაავადების სამკურნალო ეფექტს, როგორიცაა ჭრილობების შეხორცება და ქსოვილების შეკეთება.PRP-ის, უფრო კონკრეტულად, მაღალი კონცენტრაციის PGF-ის და სხვა თრომბოციტების ციტოკინების შეყვანამ შეიძლება გამოიწვიოს ანგიოგენეზი, ანგიოგენეზი და არტერიოგენეზი, რადგან სტრომული უჯრედებიდან მიღებული ფაქტორი 1a აკავშირებს CXCR4 რეცეპტორს ენდოთელიუმის წინამორბედ უჯრედებზე.ბილ და სხვ.ვარაუდობენ, რომ PRP ზრდის იშემიურ ნეოვასკულარიზაციას, რაც შეიძლება გამოწვეული იყოს ანგიოგენეზის, ანგიოგენეზის და არტერიოგენეზის სტიმულირებით.მათ ინ ვიტრო მოდელში, ენდოთელური უჯრედების პროლიფერაცია და კაპილარების წარმოქმნა გამოწვეული იყო სხვადასხვა PDG-ების დიდი რაოდენობით, რომელთაგან VEGF იყო მთავარი ანგიოგენური სტიმულატორი.კიდევ ერთი მნიშვნელოვანი და არსებითი ფაქტორი ანგიოგენეზის გზის აღსადგენად არის სინერგია მრავალ PGF-ს შორის.რიჩარდსონი და სხვ.დადასტურდა, რომ ანგიოგენური ფაქტორის თრომბოციტებიდან მიღებული ზრდის ფაქტორი-bb (PDGF-BB) და VEGF-ის სინერგიული აქტივობა განაპირობებდა ზრდასრული სისხლძარღვთა ქსელის სწრაფ ფორმირებას ინდივიდუალური ზრდის ფაქტორის აქტივობასთან შედარებით.ამ ფაქტორების კომბინირებული ეფექტი ახლახან დადასტურდა კვლევაში ცერებრალური გირაოს მიმოქცევის გაძლიერების შესახებ თაგვებში ხანგრძლივი ჰიპოპერფუზიით.
რაც მთავარია, ინ ვიტრო კვლევამ გაზომა ადამიანის ჭიპლარის ვენის ენდოთელური უჯრედების პროლიფერაციული ეფექტი და თრომბოციტების სხვადასხვა კონცენტრაცია PRP-ის მოსამზადებელი მოწყობილობის შერჩევაზე და თრომბოციტების დოზის სტრატეგიაზე და შედეგებმა აჩვენა, რომ თრომბოციტების ოპტიმალური დოზა იყო 1.5 × 10 6 თრომბოციტები/μ. 50. ანგიოგენეზის ხელშეწყობა.თრომბოციტების ძალიან მაღალმა კონცენტრაციამ შეიძლება შეაფერხოს ანგიოგენეზის პროცესი, ამიტომ ეფექტი ცუდია.
უჯრედების დაბერება, დაბერება და PRP
უჯრედის დაბერება შეიძლება გამოწვეული იყოს სხვადასხვა სტიმულებით.ეს არის პროცესი, რომლის დროსაც უჯრედები წყვეტენ დაყოფას და განიცდიან უნიკალურ ფენოტიპურ ცვლილებებს დაზიანებული უჯრედების შეუზღუდავი ზრდის თავიდან ასაცილებლად, რაც მნიშვნელოვან როლს ასრულებს კიბოს პროფილაქტიკაში.ფიზიოლოგიური დაბერების პროცესში, უჯრედების რეპლიკაციის დაბერება ასევე ხელს შეუწყობს უჯრედების დაბერებას და შემცირდება MSC-ების რეგენერაციის უნარი.
დაბერების და უჯრედების დაბერების ეფექტი
In vivo, მრავალი უჯრედის ტიპი დაბერდება და გროვდება სხვადასხვა ქსოვილებში დაბერების დროს, რომელთა შორის არის დიდი რაოდენობით დაბერებული უჯრედები.დაბერებული უჯრედების დაგროვება, როგორც ჩანს, იზრდება ასაკის მატებასთან ერთად, იმუნური სისტემის დაზიანება, ქსოვილების დაზიანება ან სტრესთან დაკავშირებული ფაქტორები.უჯრედების დაბერების მექანიზმი გამოვლინდა, როგორც ასაკთან დაკავშირებული დაავადებების პათოგენური ფაქტორი, როგორიცაა ოსტეოართრიტი, ოსტეოპოროზი და მალთაშუა დისკის გადაგვარება.მრავალფეროვანი სტიმული გააძლიერებს უჯრედების დაბერებას.საპასუხოდ, დაბერებასთან დაკავშირებული სეკრეტორული ფენოტიპი (SASP) გამოყოფს ცილოვანი უჯრედების და ციტოკინების მაღალ კონცენტრაციას.ეს განსაკუთრებული ფენოტიპი დაკავშირებულია დაბერებულ უჯრედებთან, რომლებშიც ისინი გამოყოფენ მაღალი დონის ანთებით ციტოკინებს (როგორიცაა IL-1, IL-6, IL-8), ზრდის ფაქტორებს (როგორიცაა TGF-β, HGF, VEGF, PDGF), MMP და კათეპსინი.ახალგაზრდებთან შედარებით, დადასტურდა, რომ SAPS იზრდება ასაკთან ერთად, რადგან სტაბილური პროცესი განადგურებულია, რაც იწვევს უჯრედების დაბერებას და მცირდება რეგენერაციის უნარი.კერძოდ, სახსრებისა და ჩონჩხის კუნთების დაავადებების დროს.ამასთან დაკავშირებით, იმუნური დაბერება განიხილება, როგორც მნიშვნელოვანი ცვლილება იმუნური უჯრედების სეკრეციის სპექტრში, რაც მიუთითებს, რომ TNF-a, IL-6 და/ან Il-1b კონცენტრაცია იზრდება, რაც იწვევს დაბალი ხარისხის ქრონიკულ ანთებას.აღსანიშნავია, რომ ღეროვანი უჯრედების დისფუნქცია ასევე დაკავშირებულია არაუჯრედულ ავტონომიურ მექანიზმებთან, როგორიცაა უჯრედების დაბერება, განსაკუთრებით ანთების საწინააღმდეგო და ანტირეგენერაციული ფაქტორების წარმოება SASP-ის საშუალებით.
პირიქით, SASP-ს ასევე შეუძლია უჯრედების პლასტიურობის სტიმულირება და მიმდებარე უჯრედების რეპროგრამირება.გარდა ამისა, SASP-ს შეუძლია მოაწყოს კომუნიკაცია სხვადასხვა იმუნურ მედიატორებთან და გაააქტიუროს იმუნური უჯრედები, რათა ხელი შეუწყოს დაბერებული უჯრედების კლირენსს.დაბერების უჯრედების როლისა და ფუნქციის გაგება ხელს შეუწყობს MSK კუნთების და ქრონიკული ჭრილობების შეხორცებასა და ქსოვილის რემოდელირებას.
აღსანიშნავია, რომ რიტკა და სხვ.ჩატარდა ვრცელი კვლევა და აღმოაჩინეს SASP-ის მთავარი და სასარგებლო როლი უჯრედების პლასტიურობისა და ქსოვილების რეგენერაციის ხელშეწყობაში და დაინერგა დაბერებული უჯრედების გარდამავალი მკურნალობის კონცეფცია.მათ ფრთხილად აღნიშნეს, რომ დაბერება ძირითადად სასარგებლო და აღმდგენი პროცესია.
უჯრედების დაბერება და PRP-ის პოტენციალი
ღეროვანი უჯრედების რაოდენობის შემცირებით, დაბერება გავლენას მოახდენს ღეროვანი უჯრედების მუშაობაზე.ანალოგიურად, ადამიანებში ღეროვანი უჯრედების მახასიათებლები (როგორიცაა სიმშრალე, პროლიფერაცია და დიფერენციაცია) ასევე მცირდება ასაკთან ერთად.ვანგმა და ნირმალამ განაცხადეს, რომ დაბერება შეამცირებს მყესის უჯრედების ღეროვანი უჯრედების მახასიათებლებს და ზრდის ფაქტორის რეცეპტორების რაოდენობას.ცხოველებზე ჩატარებულმა კვლევამ აჩვენა, რომ PDGF-ის კონცენტრაცია ახალგაზრდა ცხენებში მაღალი იყო.მათ დაასკვნეს, რომ GF რეცეპტორების რაოდენობის ზრდას და ახალგაზრდა პირებში GF-ს რაოდენობას შეიძლება ჰქონდეს უკეთესი უჯრედული პასუხი PRP მკურნალობაზე, ვიდრე ხანდაზმულ პირებს ახალგაზრდა ინდივიდებში.ეს დასკვნები ცხადყოფს, თუ რატომ შეიძლება იყოს PRP მკურნალობა ნაკლებად ეფექტური ან თუნდაც არაეფექტური ხანდაზმულ პაციენტებში, რომლებსაც აქვთ ნაკლები ღეროვანი უჯრედები და „უხარისხო“.დადასტურდა, რომ ხრტილის დაბერების პროცესი შებრუნებულია და ქონდროციტების დასვენების პერიოდი იზრდება PRP ინექციის შემდეგ.ჯია და სხვ.იგი გამოიყენება თაგვის კანის ფიბრობლასტების in vitro ფოტოდაბერების შესასწავლად, PRP დამუშავებით და მის გარეშე, ამ მოდელში PGF-ის საწინააღმდეგო მოქმედების მექანიზმის გასარკვევად.PRP ჯგუფმა აჩვენა პირდაპირი გავლენა უჯრედგარე მატრიქსზე, გაიზარდა I ტიპის კოლაგენი და შეამცირა მეტალოპროტეინაზების სინთეზი, რაც მიუთითებს იმაზე, რომ PRP-ს შეუძლია წინააღმდეგობა გაუწიოს უჯრედების დაბერებას და ასევე დეგენერაციულ MSK დაავადებას.
სხვა კვლევაში PRP გამოიყენეს ასაკოვანი თაგვებიდან ძვლის ტვინის დაბერებული ღეროვანი უჯრედების შესაგროვებლად.დადგინდა, რომ PRP-ს შეუძლია აღადგინოს ღეროვანი უჯრედების სხვადასხვა ფუნქციები დაბერებისგან, როგორიცაა უჯრედების გამრავლება და კოლონიების წარმოქმნა, და აღადგინოს უჯრედების დაბერებასთან დაკავშირებული მარკერები.
ახლახან ობერლორმა და მისმა კოლეგებმა ინტენსიურად შეისწავლეს უჯრედების დაბერების როლი კუნთების რეგენერაციის შესუსტებაში და შეაფასეს PRP და თრომბოციტებით ღარიბი პლაზმა (PPP), როგორც ჩონჩხის კუნთების აღდგენის ბიოლოგიური მკურნალობის ვარიანტები.მათ ჩათვალეს, რომ PRP ან PPP მკურნალობა ჩონჩხის კუნთების აღდგენისთვის დაფუძნებული იქნებოდა ბიოლოგიურ ფაქტორებზე, რომლებიც მორგებულია SASP სპეციფიკურ უჯრედულ მარკერებზე და სხვა ფაქტორებზე, რომლებიც იწვევენ ფიბროზის განვითარებას.
საფუძვლიანია ვიფიქროთ, რომ PRP-ის გამოყენებამდე, უჯრედების მიზანმიმართულ დაბერებას შეუძლია გააუმჯობესოს ბიოლოგიური მკურნალობის ეფექტურობის რეგენერაციის მახასიათებლები ადგილობრივი SASP ფაქტორების შემცირებით.ვარაუდობენ, რომ ჩონჩხის კუნთების რეგენერაციისთვის PRP და PPP მკურნალობის შედეგების გაუმჯობესების კიდევ ერთი ვარიანტია დაბერებული უჯრედების შერჩევითი მოცილება დაბერების დამცავი საშუალებებით.ეჭვგარეშეა, რომ ბოლოდროინდელი კვლევის შედეგები უჯრედების დაბერებასა და დაბერებაზე PRP-ის ეფექტის შესახებ მომხიბლავია, მაგრამ ისინი ჯერ კიდევ საწყის ეტაპზეა.ამიტომ, ამ დროს რაიმე შემოთავაზების გაკეთება მიზანშეწონილი არ არის.
(ამ სტატიის შინაარსი ხელახლა იბეჭდება და ჩვენ არ ვაძლევთ რაიმე გამოხატულ ან ნაგულისხმევ გარანტიას ამ სტატიაში მოცემული შინაარსის სიზუსტის, სანდოობის ან სისრულისთვის და არ ვართ პასუხისმგებელი ამ სტატიის მოსაზრებებზე, გთხოვთ, გაიგოთ).
გამოქვეყნების დრო: მარ-01-2023